질문 요약
5장 입체화학(4)-다양한 형태 표현 강의 중 질문이 있습니다. 두 화합물 중 첫 번째 화합물은 CH3가 후퇴, H가 전방으로 나와있는 구조(R배열)이고, 두 번째 화합물은 CH3가 전방, H가 후퇴되어 있는 형태(S배열)인데 왜 같은 화합물이라고 하시는지 설명해주시면 감사하겠습니다.
답변 요약
피셔 투영식에서 구조를 이해하려면 '수도꼭지 돌리기' 방법을 사용하면 됩니다. 2번 탄소에 있는 세 개의 치환기(메틸기, 브로민, 수소)를 기준으로, 가로줄은 돌출, 세로줄은 후퇴로 표시합니다. 이렇게 보면 두 화합물은 뉴먼 투영식에서 동일하게 보입니다. 그러므로 두 화합물은 다른 이성질체가 아니라 형태가 다른 같은 화합물입니다.
Unsplash 추천 이미지 (키워드 : chemistry, organic chemistry, stereochemistry, molecular structure, Fischer projection, Newman projection )
입체화학에서 같은 화합물로 보이는 이유
입체화학은 분자의 3D 구조와 그 구조가 화합물의 성질에 미치는 영향을 연구하는 화학의 한 분야입니다. 입체화학에서 중요한 개념 중 하나는 다양한 투영식을 사용하여 분자의 입체구조를 이해하는 것입니다. 이번 포스트에서는 피셔 투영식과 뉴먼 투영식을 통해 두 화합물이 왜 같은 화합물로 보이는지 설명드리겠습니다.
피셔 투영식
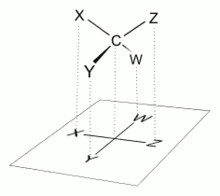
피셔 투영식은 2D 평면에 3D 구조를 나타내는 방법 중 하나입니다. 이 방법은 주로 탄소 중심에 있는 치환기들의 위치를 설명하는 데 사용됩니다. 피셔 투영식에서 가로선은 돌출된 치환기를, 세로선은 후퇴된 치환기를 나타냅니다.
뉴먼 투영식
뉴먼 투영식은 분자의 결합을 특정 방향에서 바라본 모습을 나타내는 방식입니다. 주로 두 탄소 사이의 결합을 중심으로 치환기의 상대적 위치를 설명하는 데 사용됩니다. 뉴먼 투영식에서는 앞쪽 탄소에 붙은 치환기와 뒤쪽 탄소에 붙은 치환기가 각각의 위치에 따라 서로 다른 모습을 보입니다.

화합물의 R/S 배열
입체화학에서 R/S 배열은 치환기의 우선순위에 따라 분자의 입체구조를 정의하는 방식입니다. 예를 들어, 오른쪽에 있는 화합물이 R 배열이면, 시계 방향으로 가장 높은 우선순위를 가진 치환기가 배열됩니다. 반대로 S 배열은 반시계 방향으로 배열됩니다.
이제 주어진 예제를 통해 두 화합물이 같은 화합물로 보이는 이유를 설명드리겠습니다. 주어진 두 화합물 중 첫 번째 화합물은 CH3가 후퇴하고 H가 전방으로 나와 있는 구조(R 배열)이며, 두 번째 화합물은 CH3가 전방, H가 후퇴되어 있는 형태(S 배열)입니다.
수도꼭지 돌리기 방법
피셔 투영식에서 두 화합물이 동일한지 확인하기 위한 방법 중 하나는 '수도꼭지 돌리기' 방법입니다. 이 방법은 특정 중심을 기준으로 치환기를 돌려서 두 화합물의 구조가 동일한지 확인하는 것입니다.
- 첫 번째 화합물의 피셔 투영식을 그립니다.
- 두 번째 화합물의 피셔 투영식을 동일한 기준으로 그립니다.
- 두 구조를 비교하여 동일한지 확인합니다.
예를 들어, 두 번째 화합물의 피셔 투영식에서 CH3와 H의 위치를 바꾸면 첫 번째 화합물과 동일한 구조가 됩니다. 이는 두 화합물이 실제로는 동일한 입체구조를 가지며, 단지 투영식에서 치환기의 위치가 다르게 표시된 것뿐임을 의미합니다.
결론
결론적으로, 피셔 투영식과 뉴먼 투영식을 이용하면 화합물의 입체구조를 이해하는 데 큰 도움이 됩니다. 주어진 예제에서 두 화합물이 같은 화합물로 보이는 이유는 피셔 투영식에서 치환기의 위치를 적절히 바꾸면 동일한 구조가 되기 때문입니다. 따라서 두 화합물은 실제로 다른 이성질체가 아니라 형태가 다른 같은 화합물로 이해할 수 있습니다.
입체화학의 이러한 개념을 이해하면, 더욱 복잡한 분자 구조를 이해하고 그 성질을 예측하는 데 큰 도움이 될 것입니다. 추가적인 질문이나 더 알고 싶은 내용이 있다면 언제든지 질문 주세요!
유니스터디 바로가기 : https://www.unistudy.co.kr/megauni.asp
학습Q&A 바로가기 : https://www.unistudy.co.kr/community/qna_list.asp







0 댓글